Una combinación de terapia antirretroviral con edición genética y nanomedicina ha revertido la presencia de VIH en ratones de laboratorio
Cuando uno piensa en cuál es el secreto del Virus de Inmunodeficiencia Humana, tal vez se queda en un limbo al saber que el virus «se esconde» y «reaparece» sin que logremos realmente eliminarlo del organismo.
Los que leen un poquito más llegan a comprender que esto se atribuye directamente a la capacidad del virus para integrar su secuencia de ADN en los genomas de las células del sistema inmunitario, donde permanece inactivo y fuera del alcance de los medicamentos antirretrovirales.
Por eso en estos primeros días de julio, cuando se anunció la noticia de que un equipo había revertido la presencia de VIH en organismos animales usando la combinación de varias técnicas, tal vez muchos se quedaron quietos esperando que se desmintiera la noticia cuando el virus repuntara. Pero el virus no repuntó en todos los casos, y eso es un anuncio suficientemente optimista.
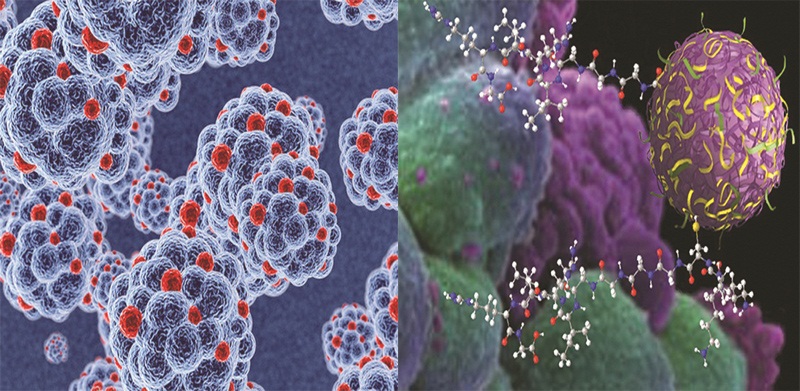
El VIH logra acceder a las células del sistema inmunitario y replicarse (izquierda). La nanotecnología emplea materiales de ingeniería que interactúan con sistemas biológicos a nivel molecular, y logran acceder a esas células.
El combo power, esa capacidad de integrar varias armas secretas para derrotar un obstáculo, no es solo una técnica de videojuegos de millenials. Llegó este julio de la mano de investigadores de la Escuela de Medicina Lewis Katz de la Universidad de Temple y el Centro Médico de la Universidad de Nebraska (UNMC), quienes lograron eliminar por primera vez del genoma de cinco ratones el VIH, según anunció la revista Science Communication, a través de dos terapias combinadas.
El paso más avanzado que tenemos hasta ahora con respecto al virus es el uso de la terapia antirretroviral, que reduce su presencia en el organismo y lo limita al interior de las células del ADN. Pero el VIH reaparece cuando esta farmacoterapia deja de administrarse, por eso no se puede hablar de cura, y la farmacodependencia es el gran obstáculo a derrotar para hallar una solución definitiva.
Usualmente, los científicos intentan el uso de una nueva terapia, o de un nuevo fármaco, sin llegar a mejores resultados.
Lo que hace especial este caso, publicado como Sequential Laser ART and Crispr Treatments Eliminate HIV-1 in a Subset of Infected Humanized Mice, es que ha aplicado no una, sino dos tipos de terapias médicas para intentar eliminar incluso las reservas del virus en sus «escondites».
La terapia antirretroviral con nanocristales (ART, por sus siglas en inglés); y la edición genética, que elimina secuencias de ADN que reproducen las enfermedades, fueron las cartas de triunfo que se integraron esta vez.
Cada una por separado, representaba una enorme ventaja, pero es el primer proyecto que las pone a trabajar juntas con el mismo fin.
Los investigadores liderados por Kamel Khalili, profesor de la Universidad de Temple, demostraron en un estudio anterior en ratas y ratones que el sistema de edición de genes podía extirpar eficazmente grandes fragmentos de ADN del VIH de las células infectadas. Pero el autor principal notó que «de manera similar a la terapia antirretroviral, la edición de genes no puede eliminar completamente el VIH por sí sola».
Para este nuevo proyecto, Khalili y sus colegas combinaron su sistema de edición de genes con el tratamiento antirretroviral, y añadieron un plus: una estrategia terapéutica reciente conocida como ART de liberación prolongada y acción lenta (Laser ART) y que fue desarrollada por el Dr. Gendelman y Benson Edagwa, especialistas de farmacología en la UNMC.
El resultado de esta integración es que se podía administrar terapia antirretroviral directamente en los reservorios «ocultos» del ADN donde el virus se esconde, a través de nanocristales que llevan el medicamento justo hasta ese lugar del organismo, y encima, la terapia de edición genética podía intentar «recortar» el ADN que ya ha sido infectado.
El resultado fue que en cinco de los ratones tratados con estas técnicas combinadas no se detectó más el virus tras los períodos de prueba.
Como valor añadido, Laser ART se dirige a los reservorios virales y mantiene la replicación del VIH a bajos niveles durante largos períodos de tiempo, esto significa que la administración de terapia antirretroviral no necesita de la frecuencia del tratamiento tradicional con pastillas.
El desarrollo de estos fármacos de larga duración fue posible gracias a cambios farmacológicos en la estructura química de los antirretrovirales, explicó National Geographic. El fármaco se empaquetó en nanocristales, que se distribuyen a los tejidos donde es probable que el VIH esté inactivo y a los que el medicamento tradicional no logra acceder.
Almacenados dentro de las células durante semanas, los nanocristales liberan lentamente el medicamento y mantienen el virus a raya durante mucho más tiempo que las usuales pastillas. Khalili explica que «queríamos ver si el Laser ART podía suprimir la replicación del VIH durante el tiempo suficiente para que Crispr-Cas9 liberara completamente a las células del ADN viral».
O sea, que mientras el virus estaba contenido por la ART con nanocristales, la terapia de Crispr-Cas 9 se encargaba de recortar las secuencias de ADN infectado definitivamente.
Pero si estamos ya pensando que las etapas de un ensayo médico son demasiado largas y habría que esperar años para ver el resultado en humanos, se nos va la mano de escépticos.
Los investigadores utilizaron ratones diseñados para producir células T humanas susceptibles a la infección por VIH, lo que permite una infección viral a largo plazo análoga a la que sufren los humanos.
De los ratones tratados con Laser ART y posteriormente con Crisp-Cas9, los análisis revelaron la eliminación completa del ADN del VIH en aproximadamente un tercio.
Lo más esperanzador de los resultados anunciados, fue la noticia de que apenas se necesita cerca de un año para intentar la prueba en humanos.
Probablemente este rango de tiempo tan corto se debe a que se trata de terapias que ya han sido probadas cada una por separado, así que el nuevo proyecto solo propone una sabia combinación de ellas, y no un tratamiento totalmente nuevo que no ha sido testeado antes.
De hecho, las potencialidades de Crispr Cas 9, la llamada técnica de «corta y pega» de la genética creada por el español Francisco Mojica, ha estado nominada al premio Nobel en Medicina y en Química, y sigue bajo la mira de especialistas de todo el mundo como una de las potentes armas médicas del futuro que es necesario afinar al máximo.
«Necesitamos la administración conjunta Laser ART como de Crispr-Cas9 para desarrollar una cura para la infección por VIH», declaró Khalili. «Sin embargo, ahora tenemos un camino claro para avanzar hacia los ensayos en primates no humanos y posiblemente ensayos clínicos en pacientes humanos en menos de un año».
Esperemos ver el trabajo en ese laboratorio, en apenas unos meses. El camino parece ser ahora la integración de las terapias de avanzada, el trabajo en equipo, eso que los gamers de hoy llaman un combo power.